
微信扫描二维码
获取公司更多资讯
公众号:viablife
欢迎您关注唯铂莱
左旋多巴——治疗帕金森的双刃剑
随着年龄的增长,人体在内外界因素的作用下,体内的组织器官会发生不可避免、逆转的改变,也就是我们常说的衰老,它是人类生命进程中的必然发展规律,在这个过程中,神经系统是受衰老影响较大的系统之一。当神经系统出现衰老现象时,容易促进神经退行性疾病的发生发展,以往通常在老龄阶段较为常见。但随着现今社会压力的逐渐增大,神经退行性疾病也普遍发生在各个年龄段,对人们的生活造成了极大的影响。
神经退行性疾病是以特异性神经元的大量丢失为主要特征的一种进行性发展的致残,严重可致死的复杂疾病,可分为急性和慢性。急性神经退行性疾病包括中风、脑损伤等,这类疾病易致残,且复发率也达到了15%以上;慢性神经退行性疾病包括阿尔茨海默病、帕金森等,这类疾病病程较长,可达数十年,其中帕金森是目前最难完全治愈的一种神经退行性疾病。
帕金森
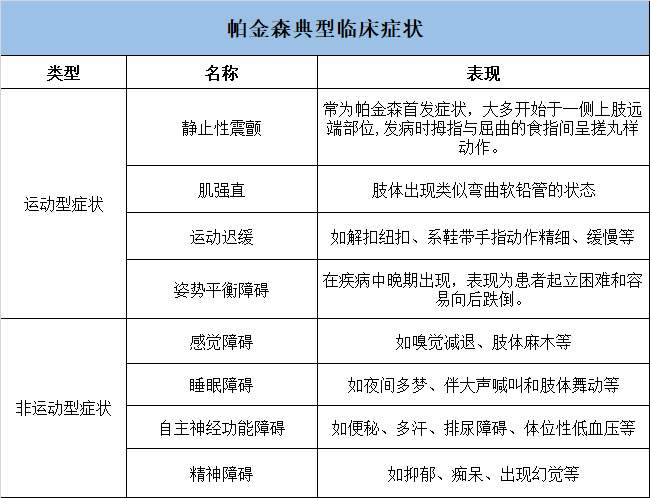
早在1817年,英国的James Parkinson医生就已经对帕金森病(Parkinson’s disease,PD)的概念、病程及特征进行了清楚地描述,PD的命名也源自于 Parkinson医生。PD也称“震颤麻痹”,是一种常见的神经退行性疾病,其典型的临床症状可分为运动型症状和非运动型症状两种类型。
PD的病因和发病机制到目前为止还没有被完全确定,但也有大量的研究推断出了可能的影响因素,包括神经元坏死、线粒体损伤、细胞自噬、免疫异常等,其中神经元坏死是相关研究人员描述最多的一种推测。

图1 神经元
神经元是神经系统最基本的结构和功能单位,分为细胞体和突起两部分,细胞体具有联络和整合输入的信息并传出相应信息的作用,而突起部分则是起到接受生物信息的功能。大量研究资料表明PD病理特征是特定蛋白质异常聚积在相关神经元的细胞体内,导致其细胞的突起部分明显变短或消亡。这种病变的神经元可长期存活,但会逐步丧失其生物功能,用目前经典的细胞死亡理论来讲,就是神经元坏死或凋亡[1]。
除了生物体内相关细胞、组织的损伤外,PD还具有一些其它的致病因素,如遗传因素,目前研究发现有10%的PD患者有家族史;环境因素也有一定的概率导致PD病发,如工业化学毒素,社会、个人因素都有可能导致神经系统病变,进而诱发PD等神经退行性疾病。
究其根本,除了发病机制无法完全确定以外,还尚未发现能够逆转或完全治愈的确切药物或疗法,导致了PD难以被完全治愈。目前对PD的临床治疗均以对症治疗为主,再辅以康复治疗,其中药物治疗是最主要的治疗手段。随着研究人员的不断探索,越来越多的PD治疗药物被开发出来,如左旋多巴、普拉克索、罗替戈汀、阿扑吗啡等[2]。
左旋多巴自20世纪60年代开始被用于治疗PD起,即被证明是治疗PD最有效的药物,不仅可改善PD患者症状,而且可以提高生活质量,因此被誉为PD治疗的“金标准”。

图2 奎奴亚藜种子
左旋多巴是可以从藜属(Mucuna sempervirens Hemsl)种子中提取出的一种氨基酸类化合物,它进入人体后,可以通过血脑屏障进入脑组织,进而发挥其药理作用。1961年,左旋多巴首次被用于PD治疗的临床试验中,并获得了明显的疗效。此后,在不断的试验中,左旋多巴逐渐成为了PD治疗的常规药物,它的加入使PD治疗领域发生了革命性的改变,改善了PD症状,降低了致残率及致死率,是PD治疗领域的一座里程碑。
到目前为止,左旋多巴仍是治疗PD的主要药物,但随着对左旋多巴的不断应用,研究人员发现长期服用左旋多巴会导致不良反应—运动并发症的发生。国内外对PD患者的多中心、横断面调查研究均表明,起病年龄早、病程长、病情严重、左旋多巴起始剂量高或高剂量长期用药都是引起运动并发症的危险因素。大数据分析显示左旋多巴用于PD治疗5~10年后,60%~90%的患者出现运动并发症;年轻发病的PD患者随病程进展,运动并发症发生率可达100%。运动并发症主要包括两种类型,一种为症状波动,如“开—关”现象(患者突然多动不安是“开”,而后又出现肌强直不能运动是“关”)等;另一种主要表现为异动症,如剂峰异动等。
针对运动并发症这一问题,研究人员从左旋多巴本身入手,提出了左旋多巴用于PD治疗的新理念。
目前有研究显示对于出现运动波动的PD患者持续静脉滴注低浓度的左旋多巴可逐渐减少运动波动,且可使“开-关”现象减少。但是长期应用这种方法会致使静脉硬化,临床实用性差,只可用于突发情况。
常规的左旋多巴药物治疗是胃肠片片剂形式的,这也导致其吸收的不稳定性,进而影响到了PD患者的症状波动,因此,改变左旋多巴的剂型是控制运动并发症的主要思路之一。
左旋多巴在单独使用的情况下,只有约1%能够进入脑内,导致其半衰期较短、生物利用度不高,于是就需要更大剂量的左旋多巴来发挥其药理作用,但是当剂量提高时,运动并发症出现的概率也会随之增长。因此,相关人员针对其半衰期短的问题进行了研究,通过联合用药/药物的方式延长了左旋多巴的半衰期,如恩他卡朋双多巴片等。

恩他卡朋双多巴片是新一代的左旋多巴复合制剂,有效成分包括左旋多巴、卡比多巴、恩他卡朋等。恩他卡朋双多巴片能够使左旋多巴的生物半衰期延长85%,生物利用度提高35%,不仅可稳定左旋多巴的血药浓度,还能使更多的左旋多巴进入脑内,从而减少左旋多巴用量,以此来减轻药物相关不良反应。
尽管长期治疗会导致运动并发症的出现,但目前左旋多巴仍然是临床上缓解PD症状的最佳治疗药物。因此,如何提供左旋多巴的最佳给药模式,保证持续性的药效,在维持疗效的同时尽可能减少运动并发症的发生,依旧是PD治疗领域不可避免的难题,这也是众多学者一直以来想要克服的。
由于尚未完全确定PD发病机制及针对性的药物或疗法,导致了完全治愈PD的困难。目前的药物治疗只能改善患者的症状,并不能从根本上去解决病因。因此,除了对现有药物进行研究改进以外,我们还需要更深入地了解PD本身,对其发病机制、影响因素、药物疗法等综合性因素进行探究,这样才能从根本上解决PD所带来的症状。
参考资料:
[1]吴卉,靳翠红.神经退行性疾病发病机制的研究进展[J].毒理学杂志,2018,32(06):484-488.
[2]李明,李秀池,肖召安.帕金森病治疗的药物选择综述[J].中国药业,2016,25(10):94-96.


